Le deep learning détecte automatiquement Six tumeurs cérébrales courantes par IRM
Une étude américaine a évalué un modèle deep learning capable d’identifier une des six tumeurs cérébrales courantes. Les résultats s’avèrent encourageant, laissant entrevoir un modèle de détection automatique de ce type de tumeurs, ainsi que l’absence d’image pathologique tumorale.
Une équipe de chercheurs américains a développé un modèle de deep learning capable de classer une tumeur cérébrale parmi l'un des six types courants, à l'aide d'une seule IRM 3D, selon une étude publiée dans Radiology: Artificial Intelligence.
Recherche sur l’automatisation de la détection des tumeurs cérébrales par deep learning
« Il s'agit de la première étude à traiter les tumeurs intracrâniennes les plus courantes et à déterminer directement la classe tumorale ou l'absence de tumeur à partir d'un volume d'IRM 3D », précise Satrajit Chakrabarty, doctorant sous la direction du Pr Aristeidis Sotiras, et du Pr Daniel Marcus, dans le laboratoire d'imagerie numérique du Mallinckrodt Institute of Radiology de la Washington University School of Medicine à St. Louis, Missouri.
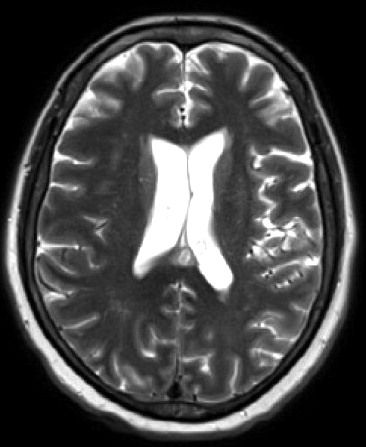 Les six types de tumeurs intracrâniennes les plus courants sont le gliome de haut grade, le gliome de bas grade, les métastases cérébrales, le méningiome, l'adénome hypophysaire et le neurinome de l'acoustique. Chacun a été documenté par histopathologie, ce qui nécessite l'ablation chirurgicale de la zone suspectée d'un cancer et son examen au microscope. Selon Chakrabarty, les approches de deep learning utilisant les données d'IRM pourraient potentiellement automatiser la détection et la classification des tumeurs cérébrales.
Les six types de tumeurs intracrâniennes les plus courants sont le gliome de haut grade, le gliome de bas grade, les métastases cérébrales, le méningiome, l'adénome hypophysaire et le neurinome de l'acoustique. Chacun a été documenté par histopathologie, ce qui nécessite l'ablation chirurgicale de la zone suspectée d'un cancer et son examen au microscope. Selon Chakrabarty, les approches de deep learning utilisant les données d'IRM pourraient potentiellement automatiser la détection et la classification des tumeurs cérébrales.
Trois groupes d’images pour tester le système
Pour construire leur modèle de deep learning, Chakrabarty et ses collègues de l'Institut de radiologie Mallinckrodt ont développé un vaste ensemble de données multi-institutionnelles d'IRM 3D intracrâniennes à partir de quatre sources accessibles au public. En plus des données internes de l'institution, l'équipe a obtenu des examens IRM préopératoires injectées pondérées en T1 à partir de la segmentation des images de tumeurs cérébrales, de l'Atlas du génome du cancer Glioblastome multiforme et de l'Atlas du génome du Gliome de bas grade du cancer.
Ils ont ainsi divisé un total de 2 105 examens en trois sous-ensembles de données : 1 396 pour la formation, 361 pour les tests internes et 348 pour les tests externes. La première série d'images IRM a été utilisée pour entraîner le réseau neuronal convolutif à faire la distinction entre les images saines et les identifications de tumeurs, et à classer les tumeurs par type. Les chercheurs ont évalué les performances du modèle en utilisant les données des IRM internes et externes.
En utilisant les données de test internes, le modèle a atteint une précision de 93,35 % (337 sur 361) dans sept groupes d’images (une classe saine et six classes tumorales). Les sensibilités variaient de 91 % à 100 %, et la valeur prédictive positive variait de 85 % à 100 %. Les valeurs prédictives négatives variaient quant à elles de 98 % à 100 % dans toutes les classes.
Des résultats fort encourageants pour une systématisation possible
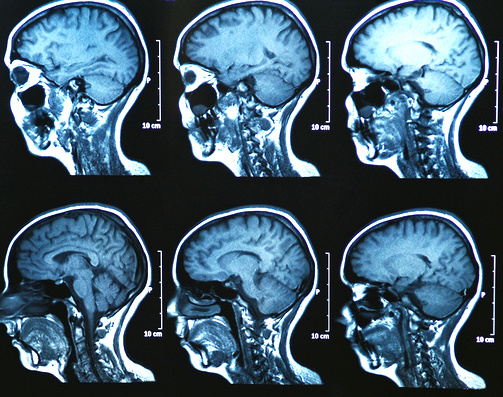 Pour l'ensemble de données de test externe, qui ne comprenait que deux types de tumeurs (gliome de haut grade et gliome de bas grade), le modèle avait une précision de 91,95 %. « Ces résultats suggèrent que le deep learning est une approche prometteuse pour la classification et l'évaluation automatisées des tumeurs cérébrales, poursuit Chakrabarty. Le modèle a atteint une grande précision sur un ensemble de données hétérogène et a montré d'excellentes capacités de généralisation sur des données de test inédites. »
Pour l'ensemble de données de test externe, qui ne comprenait que deux types de tumeurs (gliome de haut grade et gliome de bas grade), le modèle avait une précision de 91,95 %. « Ces résultats suggèrent que le deep learning est une approche prometteuse pour la classification et l'évaluation automatisées des tumeurs cérébrales, poursuit Chakrabarty. Le modèle a atteint une grande précision sur un ensemble de données hétérogène et a montré d'excellentes capacités de généralisation sur des données de test inédites. »
Il a ajouté que le modèle de deep learning 3D se rapproche de l'objectif d'un flux de travail automatisé de bout en bout en améliorant les approches 2D existantes, qui nécessitent que les radiologues délimitent ou caractérisent manuellement la zone tumorale sur une IRM avant le traitement par machine. Le réseau neuronal convolutif élimine l'étape fastidieuse et laborieuse de la segmentation tumorale avant la classification.
Le Dr Sotiras, co-développeur du modèle, a déclaré qu'il pouvait être étendu à d'autres types de tumeurs cérébrales ou troubles neurologiques, offrant potentiellement une voie pour augmenter une grande partie du flux de travail en neuroradiologie. « Ce réseau est la première étape vers le développement d'un flux de travail de radiologie amélioré par l'intelligence artificielle qui peut prendre en charge l'interprétation des images en fournissant des informations quantitatives et des statistiques », conclut Satrajit Chakrabarty.
SUR LE MÊME THÈME


Diagnostic de la SEP : une revue des critères de McDonald mis à jour en 2024
La sclérose en plaque fait l’objet de différentes formes d’apparition. Un diagnostic clinique, biologique et radiologique est établi à partir des critères de McDonald. Une revue de la mise à jour de ces critères vient d’être publiée dans l’American Journal of Roentgenology (AJR).
22/04/2026 -


L'angio-IRM objective des anévrysmes intracérébraux provoqués par une exposition répétée aux explosions
Dans un vaste échantillon de membres des forces d'opérations spéciales américaines (SOF), des chercheurs ont constaté qu'une prévalence plus élevée d'anévrismes intracrâniens était associée, de manière indépendante, à une exposition répétée plus importante aux explosions. Une étude publiée dans la r...
15/04/2026 -


Une vue d'ensemble des apports de l'échographie transcrânienne Doppler avec ou sans image
L’échographie doppler transcrânienne est aussi très pertinente sans mode B, en aveugle, pour explorer l’hémodynamique cérébrale. Un article publié dans la Revue RadioGraphics décrit une technologie, autrefois dédiée à la pédiatrie, qui a des indications pour l’exploration des adultes. Il propose une...
25/03/2026 -


Une revue des troubles dégénératifs et de leurs signes radiologiques associés
L’IRM et le TEP au FDG sont aujourd’hui à la pointe de l’imagerie pour explorer les troubles neurodégénératifs. Un article publié dans la Revue European Radiology décrit des diagnostics souvent liés à la présence d’amyloïde intracérébrale. La maladie d’Alzheimer, souvent indétectable à un stade préc...
17/03/2026 -


IRM des métastases cérébrales : le black blood et le deep learning pour optimiser l'identification des lésions
L’IRM black blood est recommandée pour mieux identifier les métastases cérébrales, en coupes fines pour ne pas passer à côté des petites lésions. Le traitement d’images aidé par le deep learning permettant d’augmenter le rapport signal/bruit dans ce cas, une étude évalue la qualité globale des image...
11/03/2026 -


Iconographie radiologique du cerveau modifié par les substances psychoactives
La Revue Radiology présente une iconographie radiologique des répercussions cérébrales de la prise régulière de substances psychoactives. Un article qui s’adresse plus particulièrement aux radiologues qui exercent aux urgences.
09/02/2026 -


Évolution de la charge de travail en neuroradiologie d'urgence depuis quinze ans
La conjoncture démographique du secteur fait craindre une surutilisation de la neuroradiologie en périodes de garde. Ce secteur, qui semble peu impacté par la hausse du nombre d’examens négatifs, fait l’objet d’une charge de travail en hausse de 130% en TDM neuroradiologique d'urgence, selon une étu...
15/01/2026 -
LETTRE D'INFORMATION
Ne manquez aucune actualité en imagerie médicale et radiologie !
Inscrivez-vous à notre lettre d’information hebdomadaire pour recevoir les dernières actualités, agendas de congrès, et restez informé des avancées et innovations dans le domaine.


